|
基于膦盐型深共熔溶剂的二氧化碳捕获在直接空气捕获过程中的分子动力学研究
*欢迎大家去观看原文,并引用 标题:Molecular Dynamics Insights of CO2 Capture through Phosphonium-Based Deep Eutectic Solvents for Direct Air Capture 期刊:ACS Sustainable Chem. Eng. 网址:https://doi.org/10.1021/acssuschemeng.4c10594
一、文章摘要负排放技术(NETs)已成为实现本代可持续发展目标的必要举措,而直接空气捕获(DAC)技术便是这一类别中的最新成员。用于 DAC 的传统胺基和碱性溶剂通常存在各种操作上的缺陷,因此,深度共晶溶剂(DESs)被视为实现这一目的的有前景的可持续替代溶剂。在本研究中,基于四丁基溴化膦(TBPBr)和三乙二醇(TEG)不同组成比例的三种 DESs通过分子动力学(MD)和密度泛函理论(DFT)进行了计算研究。这些系统基于诸如径向分布函数、组合分布函数、氢键、相互作用能和扩散行为等分子间相互作用进行分析。结果表明,长链的膦阳离子能够以笼状结构促进二氧化碳分子的移动,而 TEG 分子则因其更高的极性成为决定性因素。DES2(TBPBr与 TEG 的摩尔比为1:2)在整体上表现出更好的结构分布和对二氧化碳的亲和力,这一结果已通过 DFT研究得到证实。最后,在大气条件下(400ppm 的二氧化碳浓度)对 DES2进行了研究,以确认这种溶剂是否能够用作二氧化碳吸附剂溶剂。结果表明,该溶剂对二氧化碳分子的选择性非常出色,优于氮分子和氧分子。
二、计算图文
表 1.所研究的 DES组合情况。
表 2.利用大气二氧化碳构建 DES系统的构成
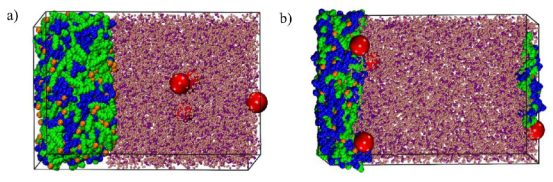
图 1.DES1(1:1)(a)之前(b)之后;DES2(1:2)(c)之前(d)之后;DES3(1:4)(e)在100 纳秒的生产运行期间之前(f)之后(蓝色 - TBPBr,绿色 - TEG,红色 - CO2)。
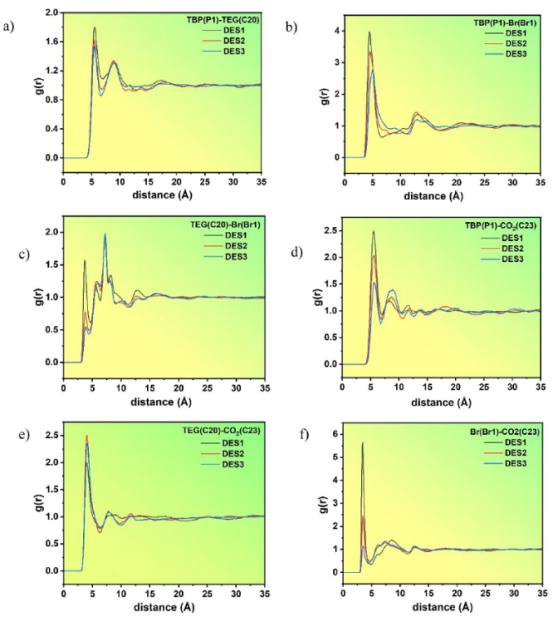
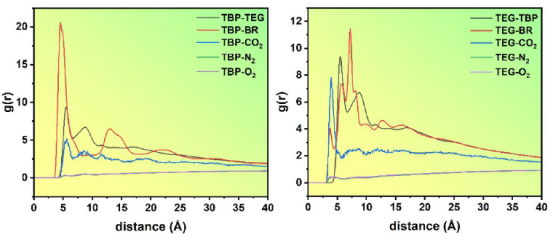
图2.三种不同 DES 的原子特异性径向分布函数对比;(a)TBP(P1)和 TEG(C20);(b)TBP(P1)和 BR(Br1);(c)TEG(C20)和 BR(Br1);(d)TBP(P1)和 CO2(C23);(e)TEG(C20)和 CO2(C23);(f)Br(Br1)和 CO2(C23)。
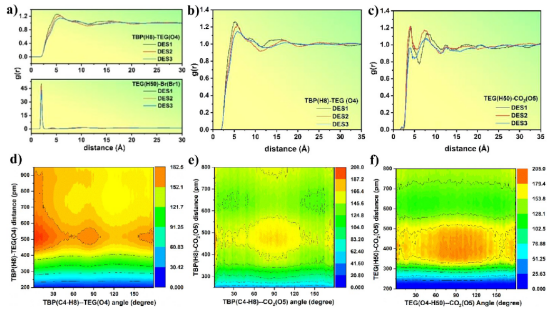
图3. DESs终端分子的 RDF 图:(a)TBP(H8)-TEG(O4) 和 TEG(H50)-Br(Br1);(b)TBP(H8)-CO2(O5);(c)TEG(H50)-CO2(O5);对应的 DES2 的 CDF 图;(d)TBP-TEG;(e)TBP-CO2;(f)TEG-CO2。
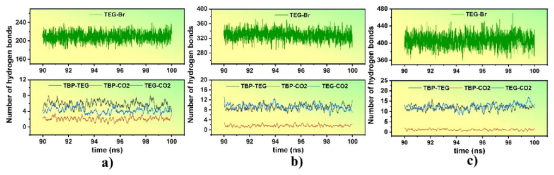
图 4.三种不同 DES系统中分子间平均形成的氢键数量:(a)DES1;(b)DES2;(c)DES3。
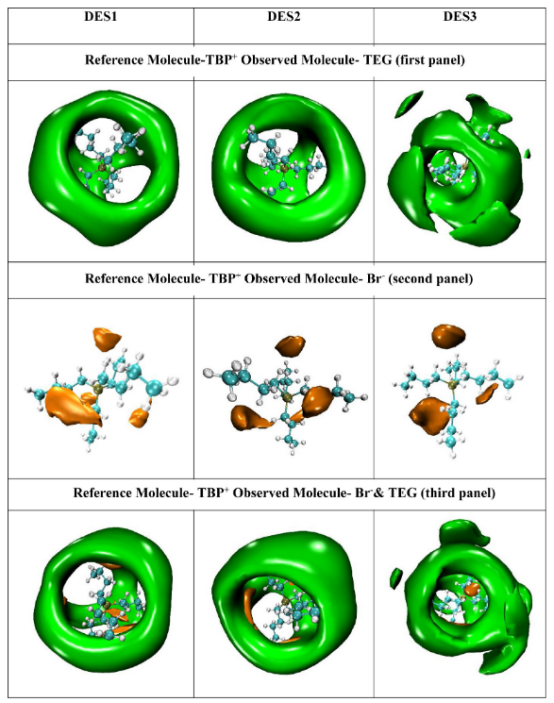
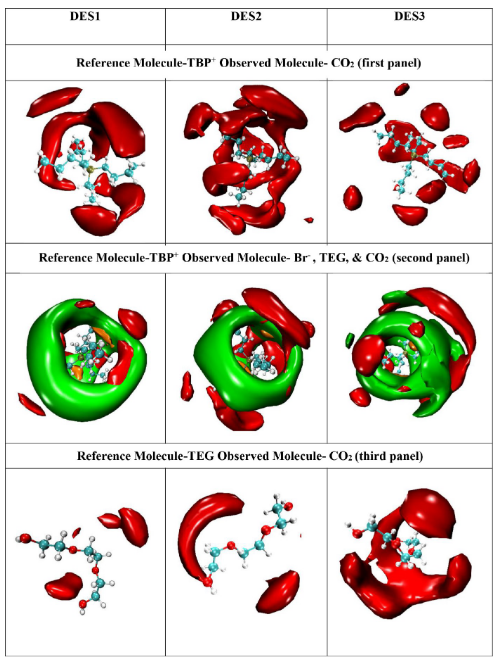
图 5.TEG 的 SDF(表面密度函数),以 TBP+作为参考分子,用于三种不同的 DES(表面等离子体共振)分析。
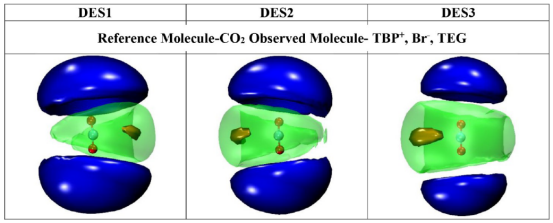
图 6.二氧化碳在 TBP+离子和 TEG 分子周围的表现形式。
图7.氢硼酸根离子、阳离子以及硼酸二酯分子在二氧化碳周围形成的吸附能图
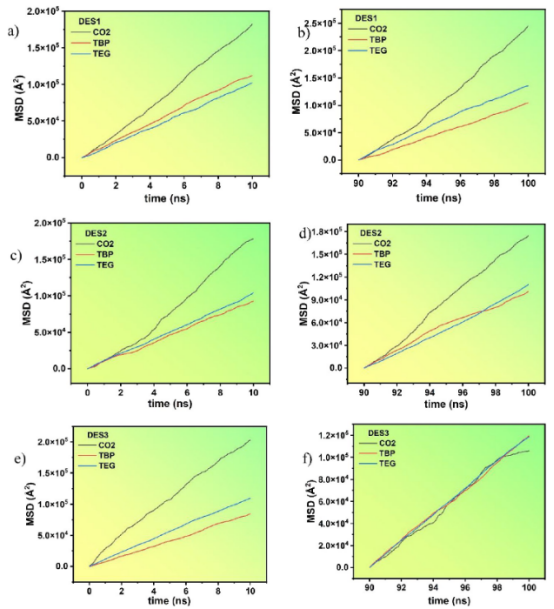
图8. (a)DES1 在10纳秒时的均方位移曲线,(b)DES1 在100 纳秒时的均方位移曲线,(c)DES2 在10纳秒时的均方位移曲线,(d)DES2 在100 纳秒时的均方位移曲线,(e)DES3 在10纳秒时的均方位移曲线,以及(f)DES3 在100 纳秒时的均方位移曲线。
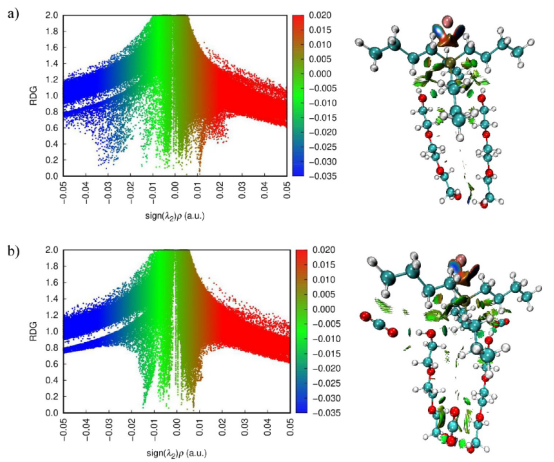
图9. (a)DES2 分子的散点图以及 RDG等值面,以及(b)在 B3LYP/6−311 + G(d,p)理论水平下存在 CO2条件下 DES2 分子的散点图以及 RDG等值面。
图10. DES2(a)在常压条件下生产运行100 微秒前(b)运行100 微秒后的状态;(蓝色 - TBP+,黄色 - Br−,绿色 - TEG,红色 - CO2,粉色 - N2,紫色 - O2)。
图 11.将 DES2 中 HBA(TBP) 和 HBD(TEG) 的原子特异性径向分布函数与溶质进行比较。
三、计算分析3.1. 溶剂结构与分布分析目的:揭示DESs的微观构型及CO₂在溶剂中的分布模式。 分析方法: 径向分布函数(RDF):量化了原子间距离与配位数,用于解析DES组分(如四丁基溴化磷TBPBr、三乙二醇TEG)之间及与CO₂的相互作用。例如,TBP⁺的烷基链形成笼状结构,促进CO₂捕获(图2显示TBP(P1)-CO₂(C23)距离约5.57 Å)。 空间分布函数(SDF):可视化分子密度分布,证实TBP⁺的笼状结构及TEG的极性位点对CO₂的亲和性(图5-7展示CO₂在TBP⁺和TEG周围的密集分布)。 组合分布函数(CDF):结合径向与角度分布,验证氢键缺失(如TBP⁺-TEG角度<90°,排除氢键主导)。
关键发现: TBP⁺的长烷基链创建“笼状结构”,容纳CO₂在终端烷基链附近(自由体积效应)。 TEG的羟基(-OH)是CO₂主要活性位点(RDF显示TEG(C20)-CO₂(C23)距离约4.02 Å,配位数高)。 DES2(TBPBr:TEG = 1:2)结构最优,CO₂分布更均匀。
3.2. 分子间相互作用与能量分析目的:量化DESs与CO₂的非共价相互作用,评估溶剂稳定性与捕获效率。
分析方法: 非键相互作用能:通过NAMD能量插件计算范德华(vdW)和静电相互作用能(表4)。例如,TBP⁺-CO₂的总能约-1.45 kcal/mol(DES1),主导为vdW力。 氢键分析:使用VMD的HBonds插件(cutoff: 3 Å, 角度180°),统计平均氢键数(图4和表S3)。Br⁻-TEG氢键主导(DES2平均329.02个)。 非共价相互作用(NCI):基于DFT的RDG分析(图9),解析作用力类型(如vdW主导CO₂吸收)。
关键发现: CO₂捕获主要由vdW力驱动(非化学吸附),利于溶剂再生。 TEG的极性增强CO₂亲和性(DES2中TEG-CO₂静电能为-0.787 kcal/mol)。 DES2相互作用能最优(总非键能-31.529 kcal/mol),稳定性高。
3.3. 动态行为与扩散分析目的:评估分子流动性及CO₂在溶剂中的传输机制。 分析方法: 均方位移(MSD)曲线:基于Einstein方程计算自扩散系数(图8)。 扩散系数计算:通过MSD斜率拟合(表5),比较不同分子在10 ns和100 ns的扩散变化。
关键发现: CO₂扩散最快(DES1中4.17×10⁻⁹ m²/s),但TEG浓度过高(DES3)会抑制扩散(因氢键增加)。 DES2扩散平衡性好(CO₂扩散系数变化仅-4.60%),支持高效捕获。
3.4. DAC条件下性能验证目的:测试DESs在低浓度CO₂(400 ppm)下的选择性与适用性。 分析方法: 大气条件模拟:构建DES2与空气组分(CO₂: 5分子, N₂: 9875分子, O₂: 2625分子)的MD系统(表2),NVT系综(150×100×100 Å盒)。 结构分析:RDF和SDF显示CO₂优先吸附(图11-12),N₂/O₂无显著峰。 能量与扩散:每分子相互作用能计算(表6),CO₂能效显著高于N₂/O₂。
关键发现: DES2对CO₂选择性高(TEG-CO₂能-2.503 kcal/mol,vs. N₂仅-0.099 kcal/mol)。 CO₂扩散慢(7.13×10⁻⁹ m²/s),表明有效捕获。
3.5力场参数的实验校准关键验证点: 采用GAFF力场参数前,通过密度实验验证模拟可靠性。 实验方法:使用安东帕密度仪(Anton Paar DMA 4500 M)在298 K、1 bar下测得DES2密度为 1.017 g/cm³。
模拟对比:相同条件下MD模拟值为 1.044 g/cm³,误差仅 2.7%(文档原文:"Validation of the parameters was performed by comparing the simulated density...")。 意义:确保力场能准确复现溶剂物理性质,为后续模拟提供基础。
3.6结构性质的互证分析1. 氢键作用的实验关联计算证据: MD统计显示DES2中Br⁻与TEG平均氢键数达 329.02个(表S3),主导DES形成。 RDF证实Br⁻-TEG距离仅 2.05 Å(图3a),符合氢键特征(<3 Å)。
实验支持: 文献[8,31]指出DES的氢键网络是低熔点的关键成因,本文DESs在室温下呈液态(实验未测但引用共识)。
2. CO₂捕获位点的双重验证计算发现: SDF显示CO₂密集分布于TEG羟基周围(图6第三行),RDF距离 3.98 Å(图2e)。 NCI分析(图9b)揭示TEG羟基与CO₂氧原子存在弱氢键(蓝色区域)。
实验呼应: 文献[10,11]报道含羟基DESs(如胆碱-乙二醇)的CO₂溶解度显著高于非极性溶剂,支持极性基团的关键作用。
3.7动态行为的间接实验关联1. 扩散系数的合理性验证模拟结果: DES2中CO₂扩散系数为 3.04×10⁻⁹ m²/s(表5),接近典型离子液体(文献[33]报道~10⁻⁹ m²/s级)。
实验对照: 文献[11]实测磷基DESs的CO₂扩散时间为分钟级,与模拟量级一致,证实传输机制可靠性。
2. DAC选择性的间接证明模拟设计: 构建含 400 ppm CO₂ 的大气系统(表2),模拟显示DES2对CO₂亲和力显著高于N₂/O₂(能量差10倍,表6)。 实验关联: 虽无直接实验,但碱性溶剂(如KOH)在真实DAC中已证明对低浓度CO₂的选择性,原理相似(静电/极性作用)。
3.8能量与溶解度的理论-经验关联计算数据: DES2的CO₂相互作用能达 -2.503 kcal/mol(TEG-CO₂,表6),主导为vdW力。 实验规律: 文献[9,30]证明物理吸附型溶剂(如硅胶)再生能耗低于化学吸附剂,与本文"可逆捕获"结论一致。
四、计算方法4.1分子动力学(MD)模拟方法与参数1. 初始系统构建分子优化: 工具:Gaussian 09,B3LYP/6-311G(d,p)理论水平。 步骤:对TBPBr、TEG、CO₂分子进行几何优化,原子标注见Figure S1。 电荷分配: 方法:限制性静电势(RESP)方法(AMBER 14)。 输出:原子部分电荷(表S1),例如Br⁻电荷为-1.0,TEG羟基氢电荷为+0.4456。 力场参数: 力场:广义Amber力场(GAFF),通过ANTECHAMBER生成。 验证:模拟DES2密度(1.044 g/cm³)与实验值(1.017 g/cm³)误差<3%,验证力场可靠性。
2. 模拟流程与系综设置软件:NAMD 2.10。 关键参数:
模拟步骤: 最小化:共轭梯度法(2 ns),消除原子冲突。 加热:0 K → 298.15 K(0.5 ns)。 平衡:NPT系综(5 ns,1 bar, 298.15 K),稳定密度。 生产运行:NVT系综(100 ns),轨迹每5 ps保存。 重复性:3组独立初始构型,确保统计显著性。
3. 特殊系统构建(DAC条件)大气模拟:400 ppm CO₂(5分子) + N₂(9875分子) + O₂(2625分子)。 挑战:低密度空气导致NPT不稳定 → 改用NVT系综。 盒尺寸:150×100×100 Å(表S2),容纳近1.3万分子。
4.2DFT计算与非共价相互作用(NCI)分析1. DFT参数设置工具:MultiWFN软件包。 理论水平:B3LYP/6-311+G(d,p)(比MD优化基组更大,提高精度)。
分析内容:还原密度梯度(RDG)与非共价相互作用可视化。 作用:区分vdW(绿色)、氢键(蓝色)、排斥(红色)区域。
2. 关键发现CO₂与TEG间存在弱氢键(蓝色小区域),主导力为vdW(绿色区域)。 TBP⁺烷基链提供疏水口袋,促进物理吸附。
4.3分析方法与验证1. 结构分析工具径向分布函数(RDF): 工具:VMD内置计算。 关键结果:TEG(C20)-CO₂(C23)距离≈4.02 Å(图2e),表明TEG是主要活性位点。 空间分布函数(SDF): 工具:TRAVIS软件。 输出:3D密度分布(图5-7),证实TBP⁺的笼状结构。
2. 动态行为量化均方位移(MSD): 计算:VMD的Einstein扩散工具(图8)。 输出:自扩散系数(表5),如DES2中CO₂扩散系数=3.04×10⁻⁹ m²/s。
氢键统计: 工具:VMD的HBonds插件。 参数:距离cutoff=3 Å,角度cutoff=180°(标准氢键定义)。 输出:DES2中TEG-Br氢键数平均329个(表S3)。
3. 能量计算非键相互作用能: 工具:NAMD Energy插件(VMD)。 分解:范德华(EvdW)与静电(Eelec)分量(表4)。 关键结果:DES2中TEG-CO₂总能量=-0.783 kcal/mol(物理吸附主导)。
|